Dwutlenek węgla (CO₂), nazywany również tlenkiem węgla(IV), to gaz powstający jako produkt całkowitego spalania substancji, których głównym składnikiem jest węgiel. Jest to związek chemiczny występujący w przyrodzie w formie cząsteczek o wzorze sumarycznym CO₂. Tlenek węgla(IV) w warunkach normalnych jest gazem i stanowi ważny składnik powietrza, choć w "czystym" powietrzu znajduje się go stosunkowo niewiele (około 0,04% objętości powietrza).
Właściwości Fizyczne i Chemiczne Tlenku Węgla(IV)
Tlenek węgla(IV) posiada szereg unikalnych cech. Jest bezbarwnym, bezwonnym gazem, który nie jest palny i nie podtrzymuje spalania. Jego gęstość wynosi około 1,977 g/l, co oznacza, że jest cięższy od powietrza (około 1,5 raza). W wodzie rozpuszcza się dosyć dobrze, tworząc słaby kwas węglowy. Temperatura sublimacji CO₂ to -78,5°C, co pozwala na tworzenie tzw. suchego lodu.
Wykrywanie Tlenku Węgla(IV)
Doświadczenia laboratoryjne potwierdzają, że tlenek węgla(IV) jest bezbarwnym, bezwonnym gazem, który nie jest palny i nie podtrzymuje spalania. Jego gęstość jest większa od gęstości powietrza, co można zaobserwować, gdy gaz "przelewa się" i gasi świeczki od dołu, zaczynając od najniżej położonej. Mętnienie wody wapiennej pod wpływem tlenku węgla(IV) jest reakcją charakterystyczną, pozwalającą na identyfikację tej substancji.
Tlenek węgla (IV) - właściwości #6 [ Powietrze i jego składniki ]
Naturalne Występowanie i Obieg w Przyrodzie
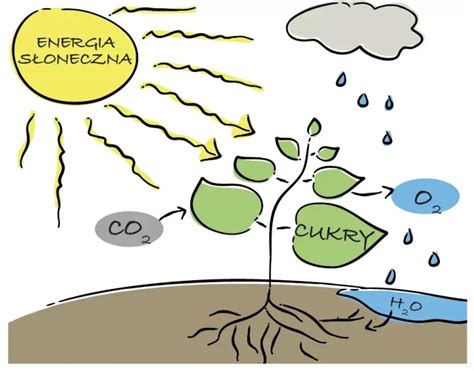
Tlenek węgla(IV) stanowi niezbędny substrat w procesie fotosyntezy. Rośliny zielone oraz niektóre bakterie przeprowadzają ten proces, w którym materia nieorganiczna (tlenek węgla(IV) i woda) zamieniana jest w materię organiczną (cukier - glukozę) z udziałem energii słonecznej. Proces ten można opisać równaniem: 6CO₂ + 6H₂O → energia, chlorofil C₆H₁₂O₆ + 6O₂.
Naturalne źródła CO₂ obejmują oddychanie komórkowe u organizmów żywych, spalanie biomasy, erupcje wulkanów oraz rozkład materii organicznej.
Zagrożenia Związane z Wysokim Stężeniem CO₂: Przykład Jeziora Nyos
Chociaż CO₂ w normalnych stężeniach atmosferycznych (około 425 ppm) nie jest trujący, to w zamkniętych przestrzeniach, przy wysokich stężeniach powyżej 5000 ppm, może powodować senność, bóle głowy i problemy z koncentracją. W skrajnych przypadkach, gdy zawartość CO₂ w powietrzu przekroczy 10%, mogą pojawić się omamy i śpiączka, a przy 20% śmierć następuje w ciągu kilkunastu minut z powodu uduszenia. Wczesnymi objawami zatrucia są osłabienie, niepokój, tętniący ból i zawroty głowy. W miarę upływu czasu pojawia się senność, apatyczność, utrata świadomości, zaburzenia oddychania i orientacji, przyspieszenie czynności serca, zaburzenia rytmu serca oraz uszkodzenie mięśnia sercowego. Następstwem ostrego zatrucia może być nieodwracalne uszkodzenie ośrodkowego układu nerwowego, niewydolność wieńcowa, zawał, a nawet śmierć.
Jedna z najbardziej tajemniczych katastrof w historii, mająca związek z dwutlenkiem węgla, wydarzyła się w nocy z 21 na 22 sierpnia 1986 r. w Kamerunie, w Afryce. W obrębie 30 km od jeziora Nyos życie straciło łącznie 1746 osób i wiele tysięcy zwierząt. Na zwłokach nie znaleziono jakichkolwiek zewnętrznych obrażeń. Osoby przybyłe nad jezioro zdziwiło obniżenie jego tafli o około metr, zmiana koloru wody z niebieskiej na czerwoną oraz drzewa leżące przy brzegu, jak po przejściu tsunami. Ci, którzy przeżyli, mieli kłopoty ze zdrowiem, mówili, że wszystkiemu winien jest duch jeziora.
Przyjmuje się, że do tej tragedii doszło na skutek gwałtownego wydzielenia się ogromnych ilości tlenku węgla(IV), nagromadzonego pod dnem jeziora. Szacuje się, że w krótkim czasie na powierzchnię wydostało się około 1,6 miliona ton CO₂. Ze względu na swoją gęstość, dwutlenek węgla wypełnił dolinę, wyparł z niej powietrze, zawierające niezbędny do życia tlen, prowadząc do śmierci przez uduszenie.

Tlenek Węgla(IV) a Tlenek Węgla(II) (Czad)
Niezwykle ważne jest rozróżnienie tlenku węgla(IV) (CO₂) od tlenku węgla(II) (CO), zwanego potocznie czadem. Są to zupełnie inne związki chemiczne o drastycznie odmiennych właściwościach i wpływie na organizm człowieka.
Czad to gaz o wzorze sumarycznym CO, który powstaje przy niecałkowitym spalaniu paliw (między innymi drewna, oleju i gazu ziemnego) oraz przy ograniczonym dostępie tlenu. Tlenek węgla(II) jest toksycznym, bezbarwnym, bezwonnym gazem, zwanym cichym zabójcą. Dostaje się do organizmu przez układ oddechowy i jest wchłaniany do krwioobiegu, blokując dopływ tlenu, gdyż tlenek węgla(II) wiąże się z hemoglobiną 210 razy szybciej niż tlen. To stwarza poważne zagrożenie dla zdrowia i życia człowieka. Każdego roku w Polsce blisko 2 tys. osób ulega zatruciu czadem, a ponad 100 z tego powodu umiera. Brak sygnałów alarmujących o jego obecności stanowi istotny czynnik przyczyniający się do zatruć.

Poniższa tabela przedstawia kluczowe różnice między tymi dwoma związkami:
| Cecha | Tlenek węgla(II) (CO) | Tlenek węgla(IV) (CO₂) |
|---|---|---|
| Stopień utlenienia węgla | +2 | +4 |
| Wzór chemiczny | CO | CO₂ |
| Toksyczność | Silnie toksyczny | Nietoksyczny w małych stężeniach, groźny w wysokich (uduszenie) |
| Źródło powstawania | Niepełne spalanie | Pełne spalanie, oddychanie, fotosynteza (substrat) |
| Gęstość względem powietrza | Nieco lżejszy | Cięższy |
Zastosowanie Tlenku Węgla(IV) jako Środka Gaśniczego
Jedną z kluczowych właściwości tlenku węgla(IV), która czyni go cennym, jest fakt, że nie podtrzymuje palenia i gasi ogień. Dzięki temu wykorzystuje się go jako środek gaśniczy w różnych typach urządzeń.
- W gaśnicach pianowych CO₂ jest stosowany jako gaz nośny, który wypycha środek gaśniczy.
- W gaśnicach śniegowych (tzw. gaśnicach CO₂) zestalony tlenek węgla(IV) (suchy lód) jest głównym środkiem gaśniczym. Wypuszczony z gaśnicy, gwałtownie sublimuje, tworząc chmurę zimnego gazu, który wypiera tlen z otoczenia ognia i jednocześnie ochładza palący się materiał.
Zdolność CO₂ do wypierania tlenu i obniżania temperatury sprawia, że jest skuteczny w gaszeniu pożarów grupy B (ciecze palne) i C (gazy palne), a także pożarów urządzeń elektrycznych pod napięciem, ponieważ nie przewodzi prądu i nie pozostawia zanieczyszczeń.

Inne Zastosowania Tlenku Węgla(IV)
Oprócz funkcji gaśniczych, tlenek węgla(IV) znajduje szerokie zastosowanie w przemyśle i codziennym życiu:
- Przemysł spożywczy:
- Do nasycania napojów gazowanych (np. wody sodowej, napojów typu cola). Technologia ta została udoskonalona przez Johanna J. Schweppe pod koniec XVIII wieku, który wykorzystał nasycenie wody dwutlenkiem węgla pod ciśnieniem.
- Jako środek konserwujący w żywności.
- W mrożeniu i schładzaniu żywności, często w postaci suchego lodu. Dzięki niskiej temperaturze przyczynia się do zahamowania rozwoju bakterii i grzybów.
- Rolnictwo: W szklarniach do wzrostu fotosyntezy, co przyspiesza wzrost roślin.
- Medycyna: W zabiegach laparoskopowych oraz do regulacji pH.
- Technologia: W procesach kriogenicznych i produkcji chemikaliów.

Otrzymywanie Tlenku Węgla(IV)
Tlenek węgla(IV) można otrzymać różnymi metodami, zarówno w laboratorium, jak i na skalę przemysłową.
Otrzymywanie w Warunkach Domowych i Laboratoryjnych
W warunkach domowych CO₂ można otrzymać poprzez zmieszanie octu (kwasu octowego, CH₃COOH) i sody oczyszczonej (wodorowęglanu sodu, NaHCO₃). Zachodzi wówczas reakcja chemiczna:
NaHCO₃ + CH₃COOH → CH₃COONa + H₂O + CO₂↑
W laboratorium tlenek węgla(IV) często otrzymuje się z reakcji węglanu wapnia (CaCO₃) z kwasem chlorowodorowym (solnym, HCl). Równanie reakcji to:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑
Inną metodą laboratoryjną jest termiczny rozkład węglanów, na przykład węglanu wapnia:
CaCO₃ → CaO + CO₂↑
Źródła Przemysłowe
Przemysłowe źródła tlenku węgla(IV) to głównie spalanie paliw kopalnych, procesy chemiczne (np. produkcja cementu) oraz karbonizacja napojów i produkcja amoniaku.