Neutrofile, stanowiące pierwszą linię obrony organizmu przed patogenami, są kluczowymi komórkami układu odpornościowego. Ich obniżona liczba, zwana neutropenią, może zwiększać podatność na infekcje. W kontekście szczepień ochronnych, szczególnie tych z użyciem szczepionek „żywych” takich jak preparat przeciwko ospie wietrznej, pojawiają się ważne pytania dotyczące bezpieczeństwa i skuteczności. Artykuł ten ma na celu przedstawienie zasad dotyczących szczepień u osób z obniżoną liczbą neutrofili, ze szczególnym uwzględnieniem szczepionki przeciwko ospie wietrznej.
Neutrofile i neutropenia: Pierwsza Linia Obrony
Rola neutrofili w układzie odpornościowym
Neutrofile są najliczniejszymi krwinkami białymi krążącymi we krwi, stanowiąc około 60-70% wszystkich leukocytów. Nazywane są również granulocytami obojętnochłonnymi lub leukocytami polimorfonuklearnymi (PMN). Komórki te posiadają segmentowane jądro, którego liczba płatów wzrasta wraz ze stopniem dojrzałości, oraz ziarnistości w cytoplazmie, zawierające białka zdolne do zabijania drobnoustrojów.
Neutrofile stanowią pierwszą linię obrony przed patogenami. Są pierwszymi leukocytami docierającymi do ogniska zapalenia, aby walczyć z drobnoustrojami poprzez fagocytozę (pochłanianie) patogenów, a także wyłapywanie ich dzięki tworzeniu tak zwanych neutrofilowych sieci zewnątrzkomórkowych.
Czym jest neutropenia?
Neutropenia to okresowe lub stałe zmniejszenie liczby neutrofili we krwi obwodowej. U dorosłych rozpoznaje się ją w przypadku obniżenia liczby neutrofili poniżej 1500/µl (1,5 G/l). Znaczne zmniejszenie liczby neutrofili poniżej 500/µl określa się jako agranulocytozę. Zbyt mała ilość neutrofili może występować samodzielnie lub towarzyszyć niedoborom czerwonych krwinek i płytek krwi, co określa się pancytopenią.
Przyczyny neutropenii
Neutropenia może mieć wiele przyczyn, które ogólnie można podzielić na wrodzone i nabyte. Neutropenia nabyta jest częściej spotykana niż wrodzona.
Neutropenia nabyta
Do najczęstszych przyczyn neutropenii nabytej zalicza się:
- Infekcje ostre i przewlekłe: głównie zakażenia wirusowe, między innymi ospa wietrzna, świnka, różyczka, grypa, a także niektóre zakażenia bakteryjne, takie jak riketsjozy, bruceloza, czy zakażenia mykoplazmą.
- Leki: przede wszystkim leki cytostatyczne, ale również wiele innych, w tym leki przeciwbakteryjne (penicyliny, chloramfenikol, sulfonamidy), przeciwtarczycowe (tiamazol), przeciwpadaczkowe (karbamazepina) i przeciwbólowe (metamizol, ibuprofen, paracetamol).
- Niedobory żywieniowe: niedobór kwasu foliowego, witaminy B12, miedzi lub jadłowstręt psychiczny.
- Choroby szpiku kostnego: zespoły mielodysplastyczne, białaczki, anemia aplastyczna, przerzuty guzów do szpiku kostnego.
- Autoimmunizacja: neutrofile są niszczone przez autoprzeciwciała. Neutropenia autoimmunologiczna może stanowić samodzielne zaburzenie lub być objawem innych chorób autoagresyjnych, np. reumatoidalnego zapalenia stawów czy tocznia rumieniowatego układowego.
- Hipersplenizm: zatrzymanie i nadmierne niszczenie krwinek w śledzionie.
Neutropenia wrodzona
Wrodzona neutropenia jest rzadsza i zazwyczaj rozpoznawana w młodym wieku. Jest uwarunkowana genetycznie i może obejmować:
- ciężką wrodzoną neutropenię (SCN),
- neutropenię cykliczną,
- neutropenię etniczną,
- zespoły niewydolności szpiku (np. niedokrwistość Fanconiego),
- zespoły przebiegające z neutropenią i niedoborami odporności (np. Zespół Chediaka-Higashiego, zespół Wiskotta-Aldricha, zespół hiper-IgM, zespół WHIM).
Objawy i diagnostyka neutropenii
Neutropenia może przebiegać bezobjawowo, na przykład w przypadku neutropenii poinfekcyjnej. Może również, szczególnie w przypadku znacznego zmniejszenia liczby neutrofili, przyczyniać się do rozwoju zakażeń bakteryjnych lub grzybiczych, włącznie z wystąpieniem sepsy. Objawy, które mogą świadczyć o neutropenii, to:
- nawracające infekcje, m.in. zapalenie zatok, płuc, ucha środkowego, skóry i tkanek miękkich,
- owrzodzenia przypominające afty w jamie ustnej (w tym na podniebieniu i języku),
- zaburzenia przyrostu masy i długości ciała u dzieci.
Neutropenia u dzieci i niemowląt
Przy rozpoznawaniu neutropenii u dzieci specjalista musi wziąć pod uwagę fizjologiczne zmiany prawidłowej liczby neutrofili we krwi. Dolna granica liczby neutrofili w zależności od wieku wynosi około:
- 1. doba życia - 6000/μl,
- 1. tydzień życia - 5000/μl,
- 2. tydzień życia - 1500/μl,
- po 2. tygodniu do 1. roku życia - 1000/μl,
- od 1. do 10. roku życia - 1500/μl,
- późniejsze lata życia - 1800/μl.
Rozpoznanie neutropenii stawia specjalista na podstawie badania morfologii krwi obwodowej z rozmazem, co pozwala określić bezwzględną liczbę neutrofili. Ocenie poddaje się również towarzyszące zmiany dotyczące krwinek czerwonych i płytek krwi. Inne badania, takie jak rozmaz krwi obwodowej, badanie szpiku, badania genetyczne czy wykrywanie autoprzeciwciał, mają na celu wykrycie przyczyny neutropenii i ewentualnego zakażenia.
Nie każda neutropenia wymaga leczenia. Neutropenia występująca w przypadku większości chorób wirusowych, trwająca 3-7 dni, zazwyczaj ustępuje samoistnie. Leczenie zależy od jej przyczyny i obecności towarzyszącego zakażenia, obejmując m.in. czynniki stymulujące kolonie granulocytów (G-CSF), antybiotyki, glikokortykosteroidy czy w rzadkich przypadkach przeszczep komórek macierzystych szpiku.
Ospa wietrzna: Choroba i jej Powikłania
Charakterystyka ospy wietrznej
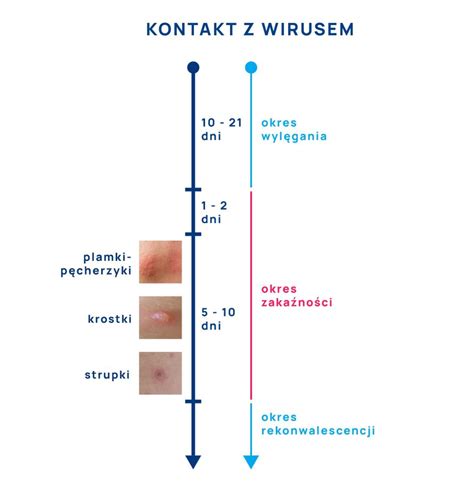
Ospa wietrzna to wysoce zakaźna choroba wirusowa wywołana przez wirus ospy wietrznej i półpaśca (VZV), który jest alfaherpeswirusem z genomem dwuniciowego DNA. Jedynym rezerwuarem wirusa jest człowiek. Pierwotny kontakt z VZV, po 10-21-dniowym okresie wylęgania, skutkuje objawami ospy wietrznej. Zakażony organizm jest niezdolny do całkowitego wyeliminowania patogenu, co prowadzi do przetrwałej infekcji w fazie latentnej w zwojach nerwowych.
Zakażenie VZV następuje drogą kropelkową lub poprzez bezpośredni kontakt z płynem wypełniającym pęcherzyki. Wirus namnaża się początkowo w nabłonku górnych dróg oddechowych i najbliżej położonych węzłach chłonnych, skąd po około 4-6 dniach trafia do krwi. Choroba rozpoczyna się od krótko trwającego okresu objawów prodromalnych, takich jak gorsze samopoczucie czy bóle mięśni, które są niespecyficznymi objawami infekcji wirusowej.
Typowe dla ospy zmiany skórne pojawiają się na owłosionej skórze głowy, twarzy i tułowiu, a następnie obejmują kończyny. Wysypka ma charakter polimorficzny - jednocześnie na skórze obecne są wykwity w różnym stadium: plamki, grudki, pęcherzyki wypełnione treścią surowiczą (z wysoką zawartością VZV), które z czasem mętnieją, tworzą pępkowate zagłębienie i przysychają w strupek. Zmiany zwykle przysychają w strupki w ciągu 7-8 dni. Rozpoznanie ospy wietrznej stawia się na podstawie charakterystycznego obrazu klinicznego.
Potencjalne powikłania ospy wietrznej
Zwykle ospa wietrzna ma łagodny przebieg, jednak może prowadzić do szeregu powikłań. Najczęściej obserwowanym powikłaniem jest bakteryjne nadkażenie wykwitów, które początkowo może obejmować powierzchniowe warstwy skóry. Jeśli jest nieleczone, może penetrować do tkanki podskórnej, prowadząc do ropowicy, a nawet martwiczego zapalenia powięzi. Dominującą florą bakteryjną są paciorkowce i gronkowce (głównie Streptococcus pyogenes oraz Staphylococcus aureus).
Do powikłań ospy wietrznej należy również zapalenie płuc, charakteryzujące się obustronnymi drobnymi guzkami w badaniu radiologicznym. Ospa wietrzna może prowadzić także do szeregu powikłań neurologicznych, takich jak ataksja móżdżkowa (najczęściej), zapalenie opon mózgowo-rdzeniowych, mózgu, rdzenia kręgowego, a także zespołu Guillaina-Barrégo czy porażenia nerwów czaszkowych. Rzadziej opisywano także powikłania w obrębie narządu wzroku, takie jak zapalenie rogówki czy martwica siatkówki, częściej u osób z niedoborami odporności.
Przykład ciężkiego przebiegu ospy wietrznej
Ciężki przebieg kliniczny ospy wietrznej związany jest z intensywnym procesem replikacji wirusa, podczas którego obserwuje się podwyższoną ciepłotę ciała, intensywny wysiew nowych zmian skórnych przez okres dłuższy niż pięć dni, a także zmiany narządowe w obrębie płuc, wątroby i ośrodkowego układu nerwowego. Przypadki o ciężkim przebiegu obserwuje się częściej u osób z pierwotnymi bądź wtórnymi niedoborami odporności, biorców przeszczepów oraz pacjentów otrzymujących leczenie immunosupresyjne.
Przykładem może być przypadek 14-miesięcznej dziewczynki przyjętej do Kliniki Chorób Zakaźnych i Neurologii Dziecięcej z powodu obrzęku i zaczerwienienia prawej kończyny górnej w przebiegu ospy wietrznej. Dziewczynka, u której pojawiły się liczne wykwity ospowe i podwyższona ciepłota ciała, rozwinęła bolesny obrzęk ręki z żółtymi strupkami. Badania laboratoryjne wykazały znaczną leukocytozę z neutrofilią oraz podwyższone wskaźniki stanu zapalnego (CRP). W wymazach ze skóry wyhodowano Staphylococcus aureus. Ostatecznie, z powodu ropowicy tkanek miękkich, konieczne było leczenie operacyjne połączone z antybiotykoterapią i leczeniem przeciwkrzepliwym. Stwierdzono również obniżenie immunoglobulin klasy G, co wymagało przetoczenia poliwalentnych immunoglobulin.
Leczenie ospy wietrznej
Znacząca większość przypadków ospy wietrznej u uprzednio zdrowych dzieci ma stosunkowo łagodny, samoograniczający się przebieg. Z tego względu leczenie u dzieci poniżej 12. roku życia, które nie chorują przewlekle, zazwyczaj jest objawowe. Odradza się stosowanie leków przeciwzapalnych, gdyż upatruje się w nich prawdopodobne hamowanie fagocytozy, a stosowanie kwasu acetylosalicylowego wiąże się ze zwiększonym ryzykiem wystąpienia zespołu Reya.
Zaleca się miejscowe stosowanie preparatów przeciwświądowych lub leków przeciwhistaminowych ogólnie (np. dimetynden, hydroksyzyna). Ważne jest skrócenie paznokci u dzieci, aby zmniejszyć ryzyko rozdrapania wykwitów i wtórnego nadkażenia. Pudry płynne na bazie cynku, choć mają zmniejszać świąd, nie wpływają istotnie na czas zasychania zmian i mogą utrudniać obserwację skóry, tworząc warunki dla rozwoju bakterii.
Leczenie przyczynowe acyklowirem, który hamuje syntezę wirusowego DNA, zalecane jest u pacjentów powyżej 12. roku życia, w przypadku powikłań lub współistnienia chorób przewlekłych, a także u dzieci z przewlekłymi chorobami układu oddechowego, ciężkimi chorobami skóry, otrzymujących glikokortykosteroidy systemowe oraz kwas acetylosalicylowy.
Szczepienia ochronne: Zasady i Typy
Mechanizm działania szczepionek
Szczepionka to preparat, którego celem jest imitowanie naturalnej infekcji i wywołanie odpowiedzi immunologicznej analogicznej do tej, która zostaje uruchomiona przez organizm podczas pierwszego kontaktu z prawdziwym mikroorganizmem (bakterią lub wirusem). Istotną różnicą jest fakt, że w przypadku szczepienia nie dochodzi do objawów typowych dla infekcji lub są one bardzo łagodne. Głównym celem szczepienia jest ochrona osoby zaszczepionej przed samą chorobą, jej ciężkim przebiegiem lub ewentualnymi powikłaniami.
Antygen, który znalazł się w organizmie na skutek szczepienia, mobilizuje komórki układu odpornościowego do produkcji swoistych przeciwciał (tzw. odpowiedź humoralna) oraz bezpośredniego zwalczania antygenu przez niektóre leukocyty (tzw. odpowiedź komórkowa). Podczas reakcji immunologicznej powstają też wyspecjalizowane komórki pamięci, które odpowiadają za długotrwały efekt szczepienia. Skuteczność szczepionki zależy nie tylko od jej składu, lecz także od sprawności układu odpornościowego oraz wieku osoby szczepionej i dobranego schematu szczepienia.
Rodzaje szczepionek
W zależności od budowy i procesu produkcyjnego wyróżnia się:
- Szczepionki żywe: zawierają całe, osłabione (atenuowane) drobnoustroje, które są w stanie rozmnażać się w organizmie osoby zaszczepionej, bez wywoływania objawów choroby. Odpowiedź immunologiczna wywołana przez ten rodzaj szczepionek jest silna, a uzyskana odporność - bardzo podobna do tej wywołanej naturalnym zakażeniem. Przykładem jest szczepionka przeciwko ospie wietrznej (VZV), MMR (odra, świnka, różyczka).
- Szczepionki inaktywowane (zabite): zawierają drobnoustroje, które zostały wcześniej zabite, lub antygeny wyizolowane z mikroorganizmów. Wywołują słabszą odpowiedź immunologiczną, co często wymaga podania kilku dawek lub substancji wzmacniających efekt (adjuwantów).
- Szczepionki wektorowe i mRNA: zawierają informację genetyczną, na podstawie której antygen jest tworzony już w organizmie osoby zaszczepionej.
Szczepienie przeciwko ospie wietrznej a neutropenia
Znaczenie szczepień w profilaktyce ospy wietrznej
Szczepionka przeciwko ospie wietrznej stanowi najskuteczniejszy sposób zapobiegania tej chorobie, a współcześnie, dzięki jej wprowadzeniu, liczba zachorowań drastycznie spadła (np. w Stanach Zjednoczonych odnotowano ponad 97% zmniejszenie liczby przypadków). Jest to szczepionka zawierająca żywy, osłabiony wirus, która zapewnia długotrwałą ochronę przed zakażeniem.
Program szczepień przewiduje podawanie dwóch dawek szczepionki dla zapewnienia optymalnej ochrony: pierwsza dawka dzieciom w wieku 12-15 miesięcy, natomiast druga dawka między 4 a 6 rokiem życia. Dwie dawki szczepionki przeciwko ospie wietrznej zapewniają około 98% skuteczność w zapobieganiu chorobie u dzieci i około 75% skuteczność u młodzieży i dorosłych. Nawet jeśli zaszczepiona osoba zachoruje, przebieg choroby jest znacznie łagodniejszy.
Profilaktyka poekspozycyjna jest kluczowym elementem zapobiegania ospie wietrznej u osób, które miały kontakt z chorym, ale same nie są odporne na wirusa. Szczepienie poekspozycyjne może być skuteczne, jeśli zostanie podane w ciągu 3-5 dni po ekspozycji na wirusa. Szczepionka przeciwko ospie wietrznej charakteryzuje się wysokim profilem bezpieczeństwa i skuteczności, a najczęstsze działania niepożądane to zaczerwienienie lub bolesność w miejscu wkłucia oraz łagodna wysypka.
Jak działają szczepionki?
Ogólne zasady szczepień u pacjentów z niedoborami odporności
Główną przyczyną zachorowań i zgonów osób z pierwotnymi niedoborami odporności (PNO) są zakażenia. Szczepienia zapobiegają wielu chorobom zakaźnym nie tylko w zdrowej populacji, lecz także wśród pacjentów z obniżoną odpornością. Podejmowanie szczepień u tych osób wymaga każdorazowo określenia przez lekarza specjalistę korzyści oraz ryzyka wynikających z planowanej procedury. Wskazania do szczepień powinny być rozważane indywidualnie w odniesieniu do konkretnej szczepionki, a zakres szczepień powinien zależeć od rodzaju choroby, typu niedoboru odporności, czasu leczenia immunosupresyjnego i czasu trwania radioterapii.
Ogólna zasada często mówi, że osobom z obniżoną odpornością nie należy podawać szczepionek „żywych”. Jest to jednak uproszczenie, a w rzeczywistości zalecenia są bardziej zniuansowane i zależą od typu niedoboru odporności.
Szczegółowe zalecenia dla pacjentów z neutropenią
Pacjenci z neutropenią, będącą formą wrodzonego lub nabytego niedoboru odporności, wymagają szczególnej uwagi w kontekście szczepień. Kluczowe jest rozróżnienie pomiędzy typami neutropenii i towarzyszącymi jej niedoborami odporności.
- Wrodzone niedobory liczby i funkcji komórek fagocytarnych (w tym neutropenia):
- Żywe szczepionki bakteryjne (np. BCG przeciwko gruźlicy, przeciwko durowi brzusznemu) są przeciwwskazane.
- Żywe szczepionki wirusowe, takie jak szczepionka przeciwko ospie wietrznej (VZV) oraz MMR (przeciw odrze, śwince i różyczce), są uznawane za bezpieczne i skuteczne, pod warunkiem, że funkcja limfocytów T jest zachowana.
- Łagodna przewlekła neutropenia u dzieci:
- Jeśli u pacjenta udokumentowano zdolność do wyrzutu granulocytów (neutrofili) do wartości >1000/µl, na przykład w trakcie infekcji, szczepienia należy realizować w zakresie poszerzonym o wszystkie rekomendowane, z użyciem zarówno preparatów inaktywowanych, jak i żywych.
- U dziecka z rozpoznaniem przewlekłej neutropenii, które jest klinicznie zdrowe, bezwzględna liczba neutrofilów (ANC - absolute neutrophil count) może być skrajnie niska, ale nie jest to przeciwwskazaniem do aplikacji szczepionki. Brak granulocytów wyłącznie w puli krążącej nie osłabia odpowiedzi na szczepienie.
- Dzieci z rozpoznaną przewlekłą łagodną neutropenią, kwalifikowane do terapii czynnikiem wzrostu kolonii granulocytów (G-CSF), mogą i powinny być szczepione w poszerzonym zakresie w trakcie leczenia.
- Ciężka wrodzona neutropenia (SCN) i inne złożone niedobory odporności:
- Odmienne zasady szczepień dotyczą dzieci z wrodzonymi, uwarunkowanymi genetycznie neutropeniami, zwłaszcza tych, które nie odpowiadają wyrzutem granulocytów na G-CSF stosowany w wysokich dawkach. U tych chorych szczepionki żywe są na ogół przeciwwskazane.
- W przypadku braku udokumentowanego wyrzutu granulocytów do wartości >1000/µl, zaleca się odstąpienie od szczepień za pomocą żywych szczepionek.
- Decyzje dotyczące szczepień takich chorych muszą być zawsze podejmowane przez specjalistę immunologa, wakcynologa lub hematologa i są indywidualizowane w odniesieniu do choroby, obrazu klinicznego i stosowanego leczenia.
W przypadku szczepienia przeciwko ospie wietrznej, osoba z niedoborem odporności powinna unikać kontaktu z osobą zaszczepioną jedynie w sytuacji wystąpienia wysypki, do czasu zaschnięcia pęcherzyków.
Ocena pacjenta przed szczepieniem
Na szczepienia ochronne zgłaszają się z założenia opiekunowie ze zdrowymi dziećmi. Standardowa kwalifikacja do szczepienia opiera się na badaniu podmiotowym (wywiadzie) i badaniu przedmiotowym. Lekarz pyta rodzica, czy dziecko jest zdrowe, o ewentualne wcześniejsze pobyty w szpitalu, przyjmowane leki, choroby przewlekłe, niepożądane reakcje po podaniu wcześniejszych dawek szczepienia oraz opiekę specjalistyczną.
Rutynowe wykonywanie morfologii krwi obwodowej, CRP czy badania ogólnego moczu u każdego dziecka przed szczepieniem nie jest zalecane i nie ma naukowych wskazań. Badania laboratoryjne stają się uzasadnione, gdy istnieją wątpliwości co do stanu zdrowia dziecka, wynikające z wywiadu lub badania lekarskiego. Na przykład, wskazaniem do morfologii krwi obwodowej lub innych badań hematologicznych mogą być dane z wywiadu i badania przedmiotowego, takie jak informacja o mniejszej aktywności, zwiększonej senności, bladości powłok skórnych (mogące świadczyć o niedokrwistości) czy częste krwotoki z nosa, liczne podbiegnięcia krwawe i wybroczyny (mogące wskazywać na skazę krwotoczną małopłytkową).
Dla dziecka z rozpoznaniem przewlekłej neutropenii, które jest klinicznie zdrowe, nie ma potrzeby oznaczania morfologii krwi w dniu szczepienia. Niska bezwzględna liczba neutrofilów (ANC) jest w tym przypadku oczekiwana i nie stanowi przeciwwskazania do aplikacji szczepionki, jeśli taką decyzję podjął lekarz specjalista prowadzący leczenie neutropenii.
Szczepienia przeciwko COVID-19 u pacjentów z PNO
W związku z aktualną sytuacją epidemiologiczną, szczepienia przeciwko COVID-19 są ważne również dla osób z pierwotnymi niedoborami odporności (PNO), w tym pacjentów z neutropenią. Pacjenci z PNO są grupą potencjalnie narażoną na cięższy przebieg COVID-19. Obecnie dostępne szczepionki mRNA oraz wektorowe nie są szczepionkami żywymi, co sprawia, że są uznawane za bezpieczne w tej populacji. Odpowiedź na szczepienie jest zależna od rodzaju PNO, stosowanego leczenia i chorób współistniejących, dlatego wymaga indywidualnej oceny.